Qualche settimana fa ho parlato della pressione negativa come metodo per accelerare la guarigione delle ferite ad alto rischio infezione.
 Un altro approccio egualmente importante è quello basato sul laser, nello specifico la terapia laser a bassa intensità (Low-level laser therapy - LLLT) o, se vogliamo, laser freddo.
Un altro approccio egualmente importante è quello basato sul laser, nello specifico la terapia laser a bassa intensità (Low-level laser therapy - LLLT) o, se vogliamo, laser freddo.
Nonostante l'ampia gamma di utilizzi, non si tratta di una tecnica particolarmente diffusa e nota al grande pubblico. Due sono le ragioni principali: nonostante i successi manca una completa comprensione del suo meccanismo di azione a livello molecolare, cellulare e tissutale; inoltre l'alto numero di parametri di cui bisogna tenere conto per sviluppare i protocolli di trattamento (lunghezza d'onda, fluenza, tempi e numero di trattamenti, polarizzazione, etc) rende la tecnica difficilmente standardizzabile.
Ad aggiungere variabili vi è poi la progressiva diffusione dei LED come sorgenti luminose per la LLLT, più economici e capaci di emettere lunghezze d'onda simili a quelle dei laser, ma con gamma di emissione più ampia rispetto al "puro" monocromatismo della luce laser. La diffusione della tecnica, sotto il nome di terapia LED, in ambulatori di chiropratica dovrebbe mettere sull'avviso i potenziali utenti ... .
Come può la LLLT indurre una risposta biologica?
A differenza dei laser "caldi", centrati sull'effetto termico, la LLLT induce una reazione fotochimica nella cellula, nota come biostimolazione (o anche fotobiomodulazione).
La fotobiologia (vale a dire la capacità dei fotoni di produrre un effetto biologico) si basa sul principio che quando la luce colpisce delle molecole chiamate cromofori, l'elettrone esterno passa al livello superiore "eccitando" la molecola. Tale effetto è strettamente correlato alla natura quantica della radiazione elettromagnetica, per cui i fotoni sono in grado di trasferire "pacchetti discreti" di energia a molecole "ricettive", vale a dire molecole i cui elettroni necessitano di quel particolare "pacchetto" per passare allo stato eccitato. La radiazione infrarossa, meno energetica rispetto a quella del visibile, ha minor effetto eccitatorio e una maggiore capacità di indurre un effetto noto come transizione vibrazionale.
Il fenomeno è ben evidente nella fotosintesi, dove la luce "eccita" la clorofilla (batterioclorofilla nel caso dei cianobatteri, alias alghe blu-verdi), ma vale anche per le flavoproteine (coinvolte sia nella fotosintesi che nella bioluminescenza) e perfino per l'emoglobina. Il caratteristico colore associato alla presenza di questi cromofori è funzione di quali sono le lunghezze d'onda assorbite, quali riflesse e quali passano "intonse" attraverso il materiale; da qui il colore verde della clorofilla, giallo delle flavoproteine e rosso per l'emoglobina
Ci serve però un altro tassello per capire l'utilità del laser freddo in biologia e per questo bisogna introdurre un fondamentale organello presente in tutte le cellule eucariote, il mitocondrio (--> qui un articolo recente in questo blog).
I mitocondri sono le centrali elettriche della cellula eucariotica, responsabili della completa scomposizione delle molecole organiche a CO2, per produrre energia chimica sotto forma di una molecola nota come ATP. Attraverso il processo di fosforilazione ossidativa (la respirazione cellulare) gli elettroni estratti durante la scissione delle molecole organiche (ossidazione) vengono canalizzati, come un vero e proprio flusso di corrente, sulle creste della membrana interna del mitocondrio dove passano da un "complesso proteico all'altro e usati per "ricaricare" l'ATP dalle sue componenti esauste (ADP e fosfato), e infine scaricati/neutralizzati sull'ossigeno a formare acqua.
Sebbene queste osservazioni avessero fornito un utile tassello per capire il meccanismo d'azione della LLLT sui mitocondri, rimaneva da capire quale fosse al loro interno la struttura molecolare che fungeva da cromoforo, il "sensore" della luce. Il "responsabile" fu in seguito trovato nel complesso IV (alias citocromo-c ossidasi / CCO), il punto terminale della catena di trasporto degli elettroni nel mitocondrio, quello in cui avviene "l'incontro" tra elettroni ed ossigeno e protoni a formare acqua (--> figura).
Ottimo, ma questo pone una nuova domanda: cosa avviene nel CCO, e poi a valle, una volta assorbita l'energia luminosa?
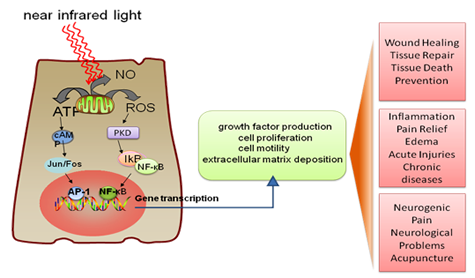
A livello cellulare, la LLLT è in grado di indurre la fotodissociazione dell'ossido nitrico (NO) dal complesso CCO. Il fenomeno è interessante in quanto le cellule sotto stress producono alti livelli di NO (grazie all'enzima NO sintasi) che va a spiazzare l'ossigeno normalmente "ospitato" dal CCO provocando così un calo nella sintesi dei prodotti chiave (ed energicamente fondamentali) della respirazione cellulare, come l'ATP.
Sommando tutti questi elementi si può capire come un trattamento laser capace di favorire la fotodissociazione del NO dal CCO, possa controbilanciare gli effetti dello stress cellulare che sono evidenti con l'accumulo di NO, ripristinando la funzionalità della centralina energetica e a cascata la produzione sia dell'ATP che di un regolatore chiave da esso derivato come l'AMP ciclico.
 Un altro approccio egualmente importante è quello basato sul laser, nello specifico la terapia laser a bassa intensità (Low-level laser therapy - LLLT) o, se vogliamo, laser freddo.
Un altro approccio egualmente importante è quello basato sul laser, nello specifico la terapia laser a bassa intensità (Low-level laser therapy - LLLT) o, se vogliamo, laser freddo.
La LLTT sfrutta un raggio laser rosso o nel vicino infrarosso (lunghezza d'onda tra 600 e 1000 nanometri) e potenza da 5 a 500 milliwatt, ed ha come caratteristica principale la non produzione di calore; da non confondere quindi con i laser usati in chirurgia per vaporizzare tessuti o cauterizzare i vasi sanguigni, la cui potenza è intorno ai 300 watt.
Tra i molteplici utilizzi del laser freddo, oltre al trattamento delle ferite, c'è quello di ausilio nel trattamento di tubercolosi, disturbi della articolazione temporo-mandibolare, affezioni muscolo-scheletriche e nella riabilitazione. Secondo alcuni è perfino utile per smettere di fumare.
Nonostante l'ampia gamma di utilizzi, non si tratta di una tecnica particolarmente diffusa e nota al grande pubblico. Due sono le ragioni principali: nonostante i successi manca una completa comprensione del suo meccanismo di azione a livello molecolare, cellulare e tissutale; inoltre l'alto numero di parametri di cui bisogna tenere conto per sviluppare i protocolli di trattamento (lunghezza d'onda, fluenza, tempi e numero di trattamenti, polarizzazione, etc) rende la tecnica difficilmente standardizzabile.
Ad aggiungere variabili vi è poi la progressiva diffusione dei LED come sorgenti luminose per la LLLT, più economici e capaci di emettere lunghezze d'onda simili a quelle dei laser, ma con gamma di emissione più ampia rispetto al "puro" monocromatismo della luce laser. La diffusione della tecnica, sotto il nome di terapia LED, in ambulatori di chiropratica dovrebbe mettere sull'avviso i potenziali utenti ... .
 |
| I diversi tipi di laser |
Come può la LLLT indurre una risposta biologica?
A differenza dei laser "caldi", centrati sull'effetto termico, la LLLT induce una reazione fotochimica nella cellula, nota come biostimolazione (o anche fotobiomodulazione).
La fotobiologia (vale a dire la capacità dei fotoni di produrre un effetto biologico) si basa sul principio che quando la luce colpisce delle molecole chiamate cromofori, l'elettrone esterno passa al livello superiore "eccitando" la molecola. Tale effetto è strettamente correlato alla natura quantica della radiazione elettromagnetica, per cui i fotoni sono in grado di trasferire "pacchetti discreti" di energia a molecole "ricettive", vale a dire molecole i cui elettroni necessitano di quel particolare "pacchetto" per passare allo stato eccitato. La radiazione infrarossa, meno energetica rispetto a quella del visibile, ha minor effetto eccitatorio e una maggiore capacità di indurre un effetto noto come transizione vibrazionale.
Il fenomeno è ben evidente nella fotosintesi, dove la luce "eccita" la clorofilla (batterioclorofilla nel caso dei cianobatteri, alias alghe blu-verdi), ma vale anche per le flavoproteine (coinvolte sia nella fotosintesi che nella bioluminescenza) e perfino per l'emoglobina. Il caratteristico colore associato alla presenza di questi cromofori è funzione di quali sono le lunghezze d'onda assorbite, quali riflesse e quali passano "intonse" attraverso il materiale; da qui il colore verde della clorofilla, giallo delle flavoproteine e rosso per l'emoglobina
Ci serve però un altro tassello per capire l'utilità del laser freddo in biologia e per questo bisogna introdurre un fondamentale organello presente in tutte le cellule eucariote, il mitocondrio (--> qui un articolo recente in questo blog).
I mitocondri sono le centrali elettriche della cellula eucariotica, responsabili della completa scomposizione delle molecole organiche a CO2, per produrre energia chimica sotto forma di una molecola nota come ATP. Attraverso il processo di fosforilazione ossidativa (la respirazione cellulare) gli elettroni estratti durante la scissione delle molecole organiche (ossidazione) vengono canalizzati, come un vero e proprio flusso di corrente, sulle creste della membrana interna del mitocondrio dove passano da un "complesso proteico all'altro e usati per "ricaricare" l'ATP dalle sue componenti esauste (ADP e fosfato), e infine scaricati/neutralizzati sull'ossigeno a formare acqua.
L'ATP può essere visto come una sorta "batteria ambulante" in quanto trasportatrice dell'energia chimica che verrà utilizzata dagli enzimi per catalizzare le innumerevoli reazioni che avvengono nei vari distretti cellulari.Esperimenti oramai classici hanno mostrato che nei mitocondri esposti ad un raggio laser (del tipo elio-neon) si aveva un aumento della respirazione cellulare (misurabile dal consumo di ossigeno) e con essa la produzione non solo di ATP e NADH, ma anche di proteine e RNA. Un effetto simile lo si ha quando un tessuto è esposto a radiazioni a bassa intensità.
Questo fatto spiega per quale motivo dosi minimali di radiazioni ionizzanti sembrano fare bene alle cellule, fenomeno come vedremo poi spiegabile con l'attivazione di meccanismi di salvaguardia della cellula. Tuttavia è bene ricordare che gli effetti delle radiazioni sono la somma di effetti deterministici (di natura fisica, con effetto proporzionale alla dose ed esistenza di soglia minima di sicurezza) e di effetti stocastici (non esiste una soglia minima in quanto l'effetto è livello genetico), quindi ogni "esposizione" alla radiazione può da un punto di vista probabilistico (di entità variabile a seconda della lunghezza d'onda) causare una mutazione.Limitandoci alle radiazioni non ionizzanti, la gamma ottimale di onde elettromagnetiche necessarie per ottenere un effetto biologico "sicuro" è quella con lunghezze d'onda comprese tra la luce visibile e l'infrarosso vicino.
Sebbene queste osservazioni avessero fornito un utile tassello per capire il meccanismo d'azione della LLLT sui mitocondri, rimaneva da capire quale fosse al loro interno la struttura molecolare che fungeva da cromoforo, il "sensore" della luce. Il "responsabile" fu in seguito trovato nel complesso IV (alias citocromo-c ossidasi / CCO), il punto terminale della catena di trasporto degli elettroni nel mitocondrio, quello in cui avviene "l'incontro" tra elettroni ed ossigeno e protoni a formare acqua (--> figura).
Ottimo, ma questo pone una nuova domanda: cosa avviene nel CCO, e poi a valle, una volta assorbita l'energia luminosa?
A livello cellulare, la LLLT è in grado di indurre la fotodissociazione dell'ossido nitrico (NO) dal complesso CCO. Il fenomeno è interessante in quanto le cellule sotto stress producono alti livelli di NO (grazie all'enzima NO sintasi) che va a spiazzare l'ossigeno normalmente "ospitato" dal CCO provocando così un calo nella sintesi dei prodotti chiave (ed energicamente fondamentali) della respirazione cellulare, come l'ATP.
Sommando tutti questi elementi si può capire come un trattamento laser capace di favorire la fotodissociazione del NO dal CCO, possa controbilanciare gli effetti dello stress cellulare che sono evidenti con l'accumulo di NO, ripristinando la funzionalità della centralina energetica e a cascata la produzione sia dell'ATP che di un regolatore chiave da esso derivato come l'AMP ciclico.
Tutto risolto?
No, in quanto bisogna sempre ricordare che la respirazione cellulare produce spontaneamente (a causa della "perdita" di alcuni elettroni che non vengono debitamente neutralizzati con la formazione di acqua dall'ossigeno) specie chimiche reattive note come radicali liberi, che la cellula cerca di tenere sotto controllo mediante processi di detossificazione. Sebbene l'azione continuativa dei radicali liberi sia alla base dell'invecchiamento cellulare, queste molecole sono funzionalmente utili, ad esempio nella difesa antimicrobica e per l'eliminazione delle cellule danneggiate, grazie anche all'attivazione di fattori proteici redox sensibili (che rilevano la variazioni dello stato di ossidazione) come NF-kB e AP-1, che a loro volta attivano a cascata geni con funzioni protettive.
No, in quanto bisogna sempre ricordare che la respirazione cellulare produce spontaneamente (a causa della "perdita" di alcuni elettroni che non vengono debitamente neutralizzati con la formazione di acqua dall'ossigeno) specie chimiche reattive note come radicali liberi, che la cellula cerca di tenere sotto controllo mediante processi di detossificazione. Sebbene l'azione continuativa dei radicali liberi sia alla base dell'invecchiamento cellulare, queste molecole sono funzionalmente utili, ad esempio nella difesa antimicrobica e per l'eliminazione delle cellule danneggiate, grazie anche all'attivazione di fattori proteici redox sensibili (che rilevano la variazioni dello stato di ossidazione) come NF-kB e AP-1, che a loro volta attivano a cascata geni con funzioni protettive.
Riassumendo il tutto, il laser freddo agisce stimolando i naturali processi di guarigione grazie alla compensazione dello stato di stress cellulare e alla attivazione di fattori di trascrizione che coordinano la risposta genica anti stress (tra cui quelli coinvolti nel processo di guarigione tissutale).


Nessun commento:
Posta un commento