Microorganismi geneticamente modificati sono da tempo usati come fabbriche viventi per produrre farmaci e prodotti chimici di qualità.
Tra le innovazioni metodologiche degli ultimi anni, di particolare interesse è quella che ha visto l'unione tra la capacità produttiva dei batteri e la tecnologia dei semiconduttori. L'obiettivo ultimo era quello di mutuare la funzione dei pannelli solari sul tetto di una casa, cioè la cattura dell'energia della luce, per alimentare la "fabbrica-batterio".
La trasformazione dell'energia elettromagnetica (luce) in energia chimica non è ovviamente una invenzione umana. Il "brevetto" appartiene agli organismi fotosintetici (dalle alghe verdi unicellulari alle piante) che usano l'energia luminosa per avviare un processo di riduzione (cioè il trasferimento di elettroni verso una molecola) che fornisce l'energia chimica per l'assemblaggio dei mattoni di carbonio (disponibili come CO2) e dell'acqua in molecole complesse come gli zuccheri (dal glucosio alla lignina) e molto altro.
I primi sistemi ibridi biologici-inorganici (bioibridi), focalizzati sulla fissazione della CO2 atmosferica e la produzione di energie alternative, sebbene promettenti, presentavano punti critici che tuttavia sono stati il punto di partenza per altre innovazioni. Ad esempio nel processo di fissazione della CO2 mediata da semiconduttori, emergeva sia il problema della tossicità da metalli per la cellula batterica, che la gamma tutto sommato ridotta di prodotti sintetizzabili. Per sfruttare al meglio la tecnologia si doveva passare a microorganismi resistenti e con un metabolismo più complesso (utilizzabile per sintetizzare una gamma di composti più ampia) e che fossero allo stesso tempo facili da maneggiare in laboratorio e crescere in un bioreattore.
Una "evoluzione" che ha dato ora i primi risultati, frutto di un lavoro di un team di Harvard pubblicato sulla rivista Science.
I ricercatori hanno scelto come microbo-fabbrica il lievito - un organismo già ampiamente usato su scala industriale e che è geneticamente facile da manipolare - "montando" sulle sue cellule dei semiconduttori capaci di fornire energia biochimica alla macchina metabolica del lievito senza però essere tossico.
Scopo della ricerca era massimizzare la capacità dei lieviti di produrre acido shikimico, un precursore di vari farmaci (tra cui l'antivirale Tamiflu).
Il lievito (Saccharomyces cerevisiae) ha una capacità intrinseca di produrre acido shikimico che usa come punto di partenza per la sintesi di elementi essenziali come proteine e altre biomolecole. In una prima fase i ricercatori hanno reso più efficiente il processo, aumentando il "rifornimento" di atomi di carbonio (derivanti dal metabolismo degli zuccheri) nel processo di sintesi della molecola, dirottati da altre vie metaboliche parallele.
Il procedimento funzionava ma presentava un problema tecnico importante. L'effetto positivo dello storno del flusso di carbonio dalle "altre" vie metaboliche andava a scapito dei processi che fornivano l'energia necessaria alla parte finale del processo di sintesi. Quindi il processo era si più efficiente nella gestione del carbonio ma creava un collo di bottiglia nell'energia disponibile (sotto forma di NADPH, molecola "depositaria" di energia chimica, essenziale per i processi anabolici) per portare a termine il processo.
La soluzione è venuta sfruttando l'approccio biobrido, basato sui semiconduttori, precedentemente testato sui batteri. In pratica è come se sulla parte esterna della cellula del lievito fossero state montati dei "pannelli solari", capaci di convertire la luce in un flusso di elettroni che veniva infine "scaricato" nella produzione di NADPH.
La scelta del semiconduttore è caduta sul fosfuro di indio assemblato perché divenisse modulare (quindi scalabile) e soprattutto non tossico per il lievito. Per farlo i ricercatori hanno rivestito le nanoparticelle di fosfuro di indio con una "colla" naturale a base di polifenoli, cosa che ha permesso da una parte di "attaccare" le nanoparticelle alla parete cellulare e dall'altra di schermare le cellule dalla tossicità del metallo.
Quando vengono esposte alla luce, le nanoparticelle raccolgono gli elettroni indotti dai fotoni e li girano nel citoplasma delle cellule di lievito, dove vengono incamerati come energia chimica in NADPH, utilizzabili nella biosintesi dell'acido shikimico, processo ora non più bloccato dal collo di bottiglia a valle.
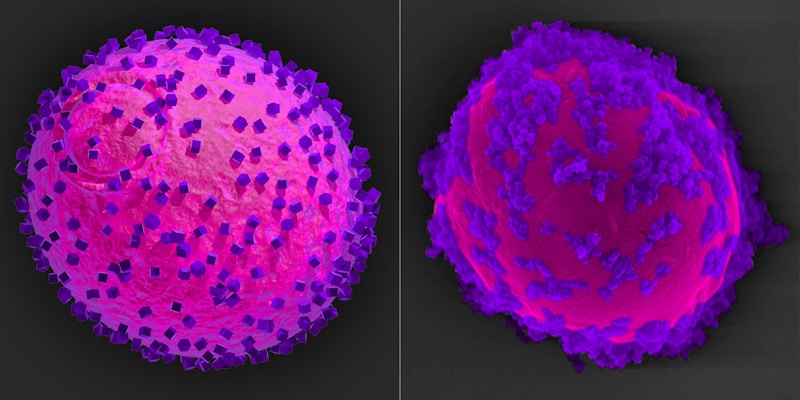 |
| L'immagine in falsi colori al microscopio elettronico di una cellula di lievito modificata. In viola sono le nanoparticelle di semiconduttore (Credit: Wyss Institute at Harvard University) |
Al buio le cellule del bioibrido di lievito hanno un metabolismo standard con la produzione di molecole organiche semplici come glicerolo ed etanolo. Una volta esposte alla luce il surplus di energia le fa passare in automatico e rapidamente alla produzione dell'acido shikimico con un aumento di 11 volte nella produzione.
L'approccio è scalabile e crea uno spazio di design completamente nuovo per le future tecnologie bioibride.
Video con la descrizione del lavoro
Light-driven fine chemical production in yeast biohybrids from Wyss Institute on Vimeo.
Video con la descrizione del lavoro
Light-driven fine chemical production in yeast biohybrids from Wyss Institute on Vimeo.
Fonte
- Light-driven fine chemical production in yeast biohybrids
J. Guo et al, Science (11/2018): 362(6416), pp. 813-816
-Solar panels for yeast cell biofactories
wyss.harvard.edu / news


Nessun commento:
Posta un commento